Biomedical Microsystems Lab
研究内容
最近の研究プロジェクトおよび研究テーマ
Advanced Microsystems
私たちの研究室では、マイクロ流体工学、集積回路、バイオテクノロジー、インフォマティクスを組み合わせて、高度なバイオメディカルマイクロシステムを開発しています。
2D Flow Cytometer
様々なサイズの細胞や細胞塊を高スループットで解析できる二次元フローサイトメーター(2DFC)の研究・開発を行っています。2DFCは、蛍光を励起光との時間領域での分離により単一光子レベルで検出可能な半導体素子であるSPAD(Single Photon Avalanche Diode)を幅の広いマイクロ流路底面にアレイ状に配置し、アレイの各点で同時並列に細胞集団からの蛍光検出を行う新概念のフローサイトメトリー技術であり、蛍光信号の時系列データを分析することで細胞を検出します。2DFCを用いることで、細胞集団の中からまれな標的がん細胞を検出することが可能になります。

Electroactive Microwell Array for Single Cell Analysis
1細胞の内物質を高効率で分析できるEMA(Electroactive Microwell Array)の研究・開発を行っています。EMAは、各マイクロウェルの下部に配置された電極を用いて、誘電泳動による1細胞捕捉と、電気穿孔法による細胞破砕が可能な技術です。EMAを用いて各細胞を単一細胞レベルでマイクロウェルに捕捉し、超微小反応体積で高精度1細胞解析が可能です。
Addressable Electroactive Microwell Array
電極の個別制御することで、細胞の高精度制御が可能なAEMA(Addressable Electroactive Microwell Array)の研究・開発を行っています。AEMAは高効率で選択的に一細胞を捕捉することができるため、順番に各々の細胞群を挿入することで単一マイクロウェルに選択的に1細胞の組み合わせを作れることが可能である。AEMAを用いて細胞間相互作用を1細胞レベルで解析しています。

Electrochemical Nanosensor
ナノサイズの電気化学センサーを用いて、量子輸送現象によるラベルフリー生化学分析が可能な電気化学ナノセンサーの研究を行っています。
Single-cell electrochemical aptasensors
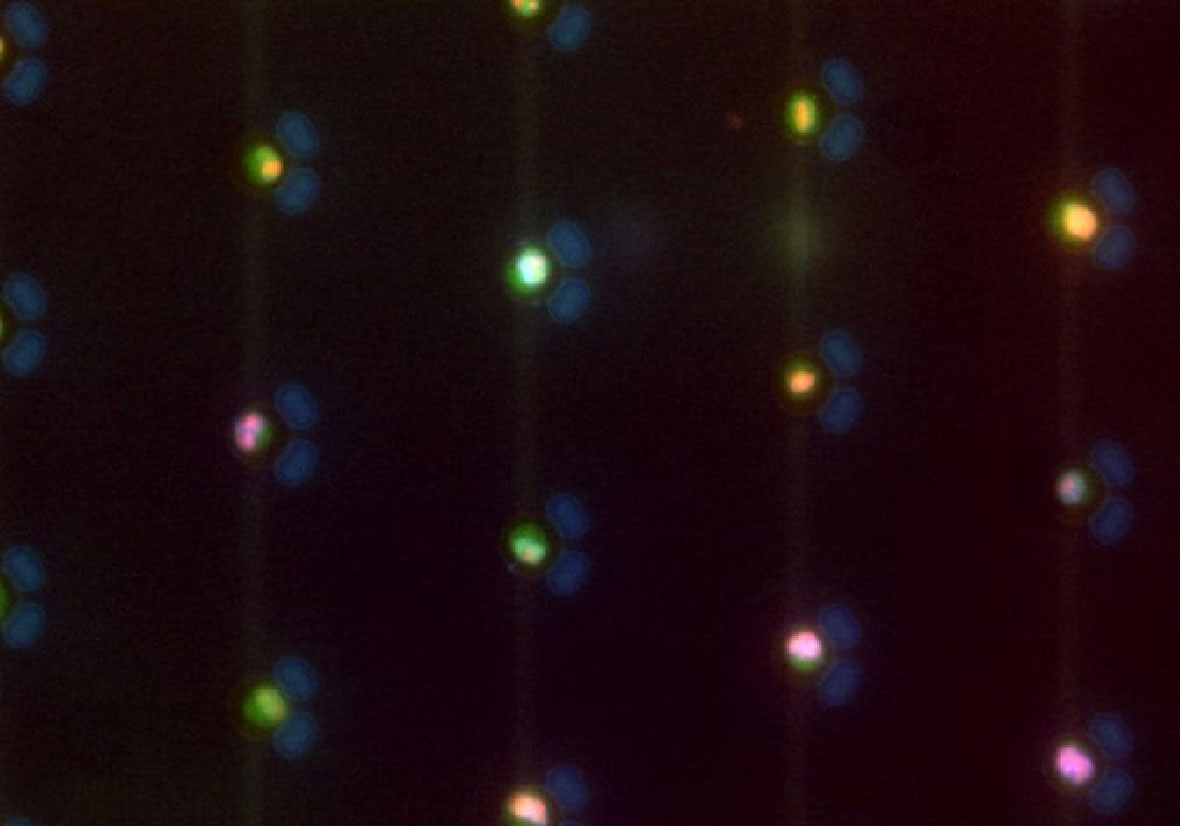
マイクロウェルの底面に固定されたフェロセン修飾DNAアプタマーを活かした1細胞電気化学センサーの研究・開発を行っています。上皮細胞接着分子(EpCAM)を標的とするアプタマーを用いた1細胞電気化学センサーアレイを用いてがん細胞の検出に成功しました。ラベルフリーでがん細胞の検出が可能な1細胞電気化学センサーを活かして、臨床環境における早期がん診断やがん治療への展開を試みています。
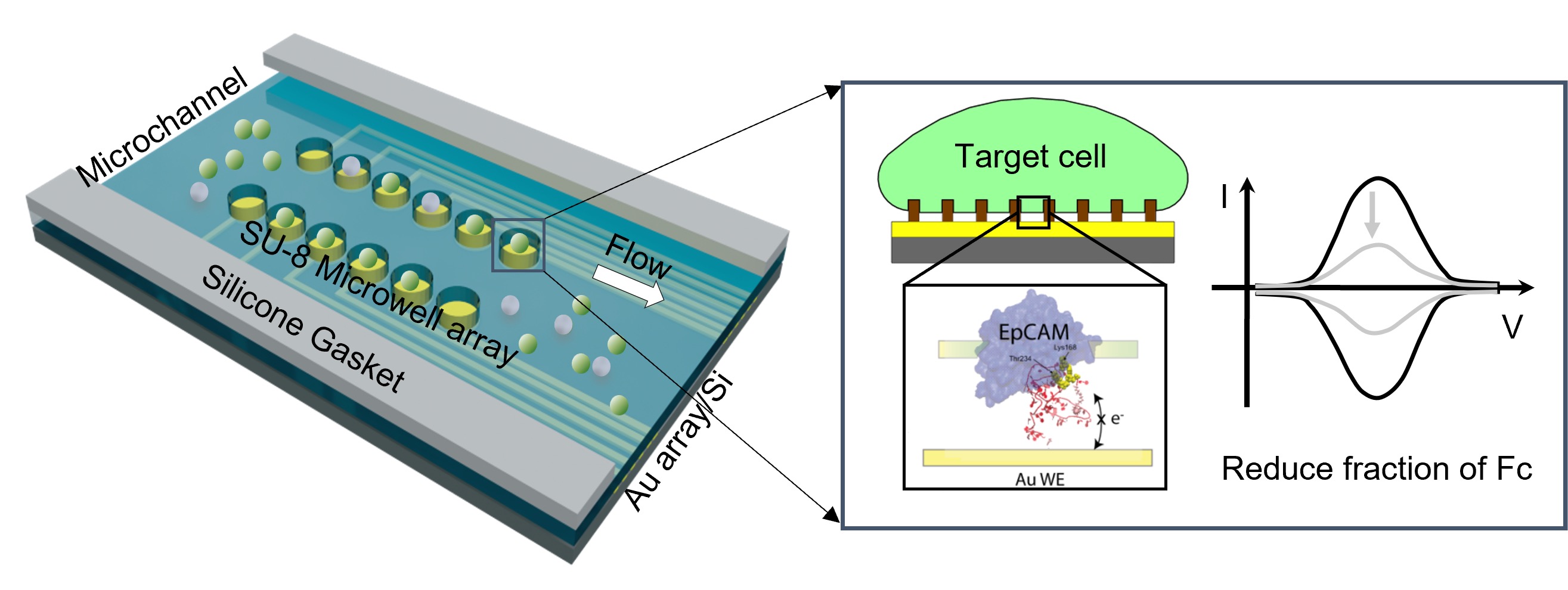
Nanotransistors sensors
高感度センシング技術である超小型ナノトランジスタと、様々な化学種を選択的に捕捉可能な人工レセプタを融合することで、複数の標的化学種を高感度で同時並列に検出できる「ナノトランジスタセンサアレイ」の研究・開発を行っています。ナノトランジスタセンサアレイを、生化学物質(サイトカイン、ケモカイン、フラクタルカイン等)の測定に応用することで細胞間伝達物質モニタリングの実現を目指しています。

Molecular and quantum (bio) electrochemistry
ショットノイズの測定や酸化還元反応による生体分子測定を利用して、量子輸送と電気化学測定の関連を明らかにするための研究を行っています。具体的には、分子動力学と単一電子計数を結合したソフトウェア(qbiol)を開発し、ナノ電気化学とナノ空間に拘束された生体分子の挙動をより深く理解し、超感度測定のための新しい方法の確立を試みています。
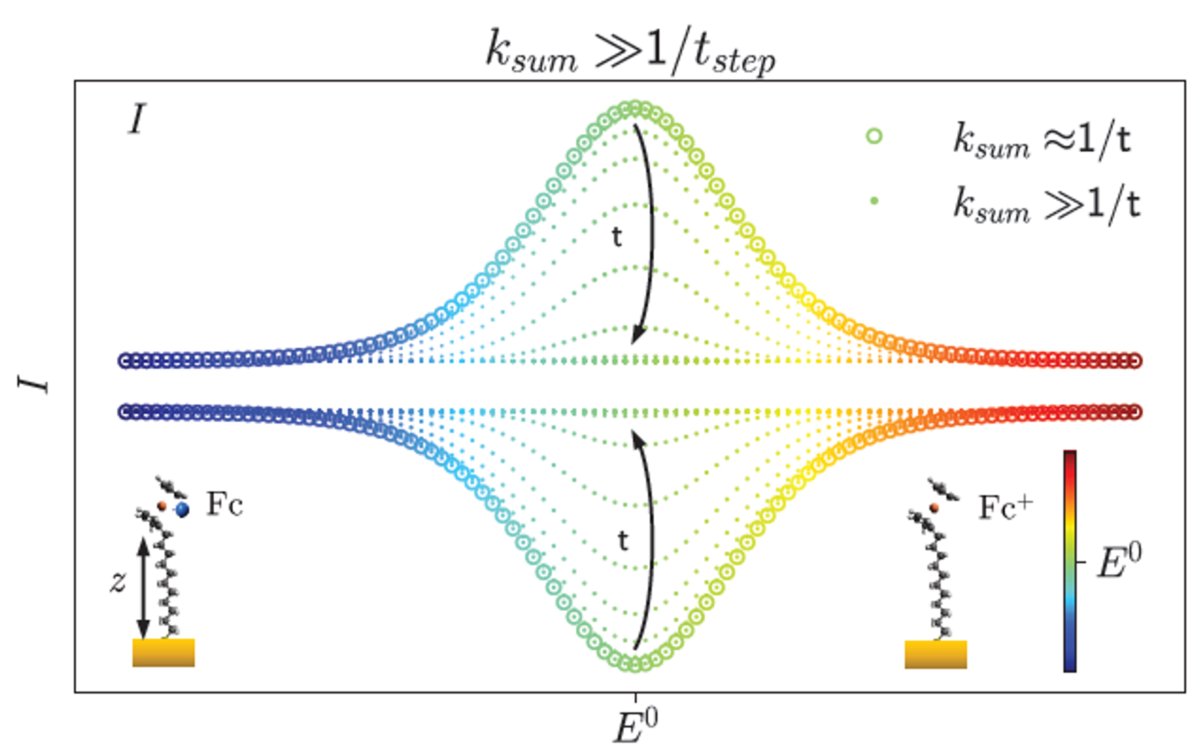
DNA Nanotechnology
DNAナノテクノロジーを活かして、分子ニューラルネットワークやDNAハイドロゲルなどの革新的なバイオメディカルシステムを構築に関する研究を行っています。
DNA hydrogel
相補的な配列とスティッキーエンド(連結用のDNA末端)を有する一本鎖DNAを用いて自己組織化が可能なDNAハイドロゲル技術を開発する。さらに、癌細胞の表面マーカーに対する抗体にスティッキーエンドをもつDNAを連結し、この周りにDNAハイドロゲルが自己組織化することで、細胞集団から癌細胞を選別的に捕獲する技術を確立する。捕獲された癌細胞に対して様々な解析を行うことで、血中の癌細胞多様性の理解を深めるとともに、血中の癌細胞を用いた癌診断・予後方法の確立を試みる。

FindCov
COVID19の世界的な大流行により、ウイルスRNAを高感度で検出することが可能な安価でシンプルな検出方法の確立が強く求められている。本研究では、DNAの相補的な配列とマイクロビーズを利用することで、酵素フリーでウイルスRNA を高感度で検出可能な技術の開発を目指している。
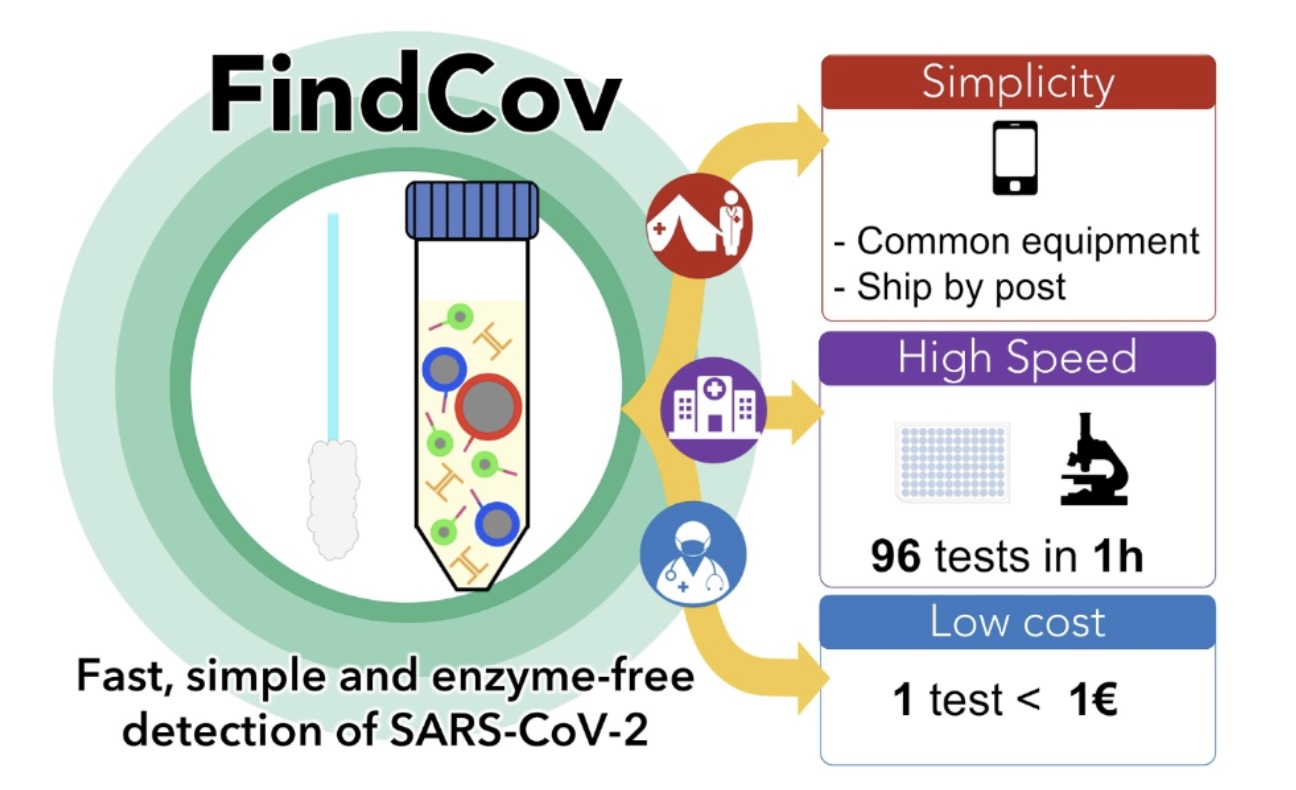
DNA conjugated nanoparticles
本研究では、DNAプログラミング方法を活かして、DNAナノ粒子の自己組織化方法を確立する。

Liquid Biopsy
血液中の腫瘍マーカーを高感度で検出可能なマイクロシステムの開発により、高精度リキッドバイオプシーの実現を目指して研究を行っています。
Circulating Tumor Cell
がんの正確な診断と予後を目指し、血液中の腫瘍マーカーである循環腫瘍細胞およびその塊を同時に捕捉し、解析可能なマイクロウェル・オン・エレクトロードアレイ(MOE)を開発しています。MOEデバイスでは、櫛型電極上に作製された細胞サイズのマイクロウェルを用いて細胞やその塊をひとつずつ捕捉することが可能になります。このMOEデバイスと、物理的および生化学的特性に基づく多特性分離方法とを組み合わせることで、がん患者血液中の循環腫瘍細胞およびその塊を同時に捕捉し、その多様性を解析することで、高精度なリキッドバイオプシーの実現を目指しています。
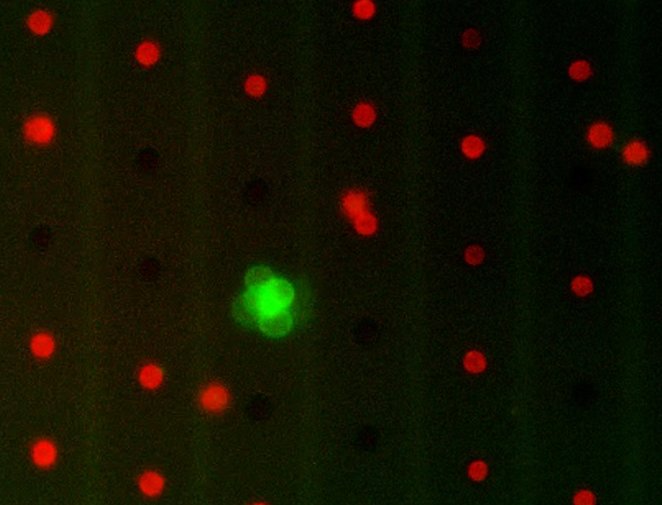
Circulating Tumour DNA
DNA断片を高効率で捕捉可能なDNA捕捉ビーズを用いて、循環腫瘍DNA(ctDNA)の超高感度検出のための新しいデジタルPCRアプローチを確立しています。具体的には、DNA捕捉ビーズにDNA断片を捕捉することでDNA断片を濃縮し、油中水滴を用いてDNA捕捉ビーズの区画化を行うことで、デジタルPCRによる超高感DNA検出が可能になります。このシステムをがん患者血液中のctDNA検出に応用することで、がんの初期診断や正確な予後への応用が期待できます。
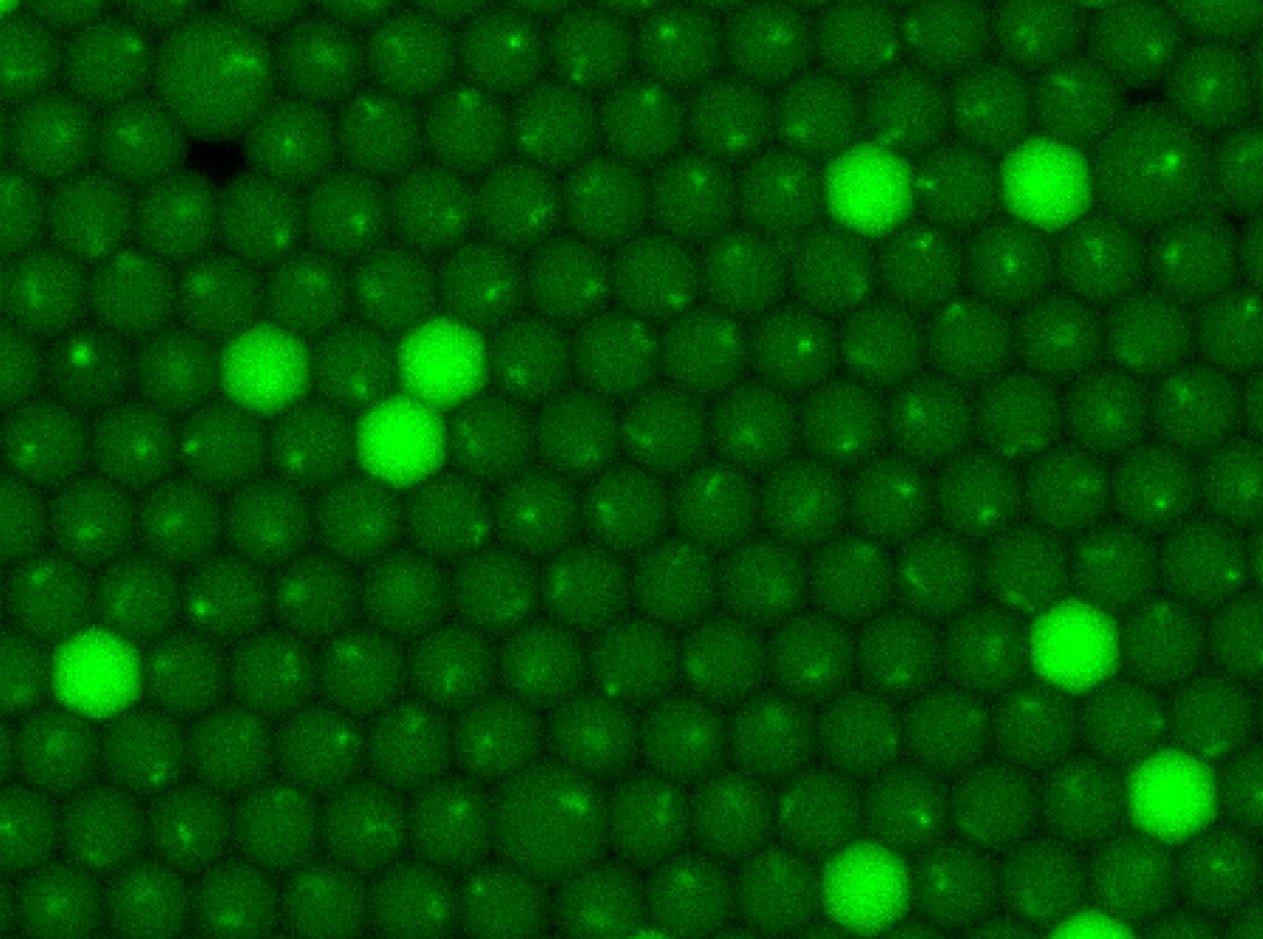
Exosome
ピコリアクターの超微細反応体積を活かして、単一エキソソームの解析が可能なマイクロシステムを開発しています。単一エキソソーム内部RNAのトランスクリプトーム解析を行うことで単一エキソソームの性質を把握することが可能になります。
